INDIKATOR ASAM BASA
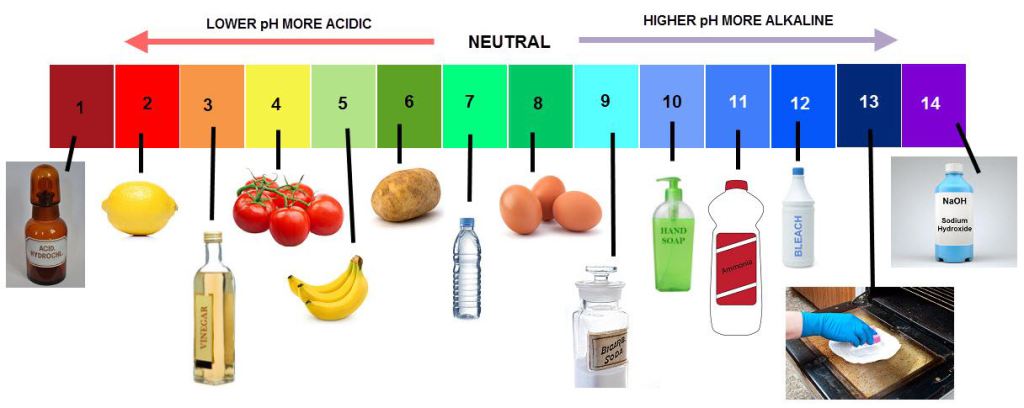
Untuk mengetahui nilai pH suatu larutan dapat dilakukan dengan menggunakan pH meter atau Indikator asam basa. pH meter merupakan suatu rangkaian elektronik yang dilengkapi dengan elektrode kaca. Jika elektrode kaca ini di masukkan ke dalam larutan, akan timbul beda potensial yang diakibatkan oleh adanya ion H+ dalam larutan. Besarnya beda potensial ini ditunjukkan dengan angka yang menyatakan pH larutan tersebut.
Alat ini mengukur berdasarkan perbedaan relatif konsentrasi ion H+. Oleh karena itu, setiap kali melakukan pengukuran pH meter harus dikalibrasi menggunakan larutan yang sudah diketahui pH-nya dengan pasti. Untuk menggunakan alat ini cukup dengan mencelupkan elektrodenya ke dalam larutan yang diukur dan secara otomatis jarum penunjuk atau angka digital akan menunjuk pada nilai pH larutan yang diukur.
Indikator asam basa adalah suatu zat yang mempunyai warna tertentu pada pH tertentu. Sebagai contoh, bromtimol biru (BTB) akan berwarna kuning dalam lingkungan asam, berwarna biru dalam basa, dan berwarna hijau pada suasana netral.
Ditinjau dari senyawanya, indikator asam basa merupakan zat warna yang dianggap sebagai asam lemah (HIn) dalam larutan dan terionisasi menghasilkan ion H+.
HIn(aq) H+(aq) + In–(aq)
Warna Hin berbeda dengan warna In–. Pada pH = pKa atau [H+] = Ka indikator, maka [In–] sama dengan [HIn] sehingga yang tampak adalah warna campuran antara warna HIn dan warna In–. Pada pH lebih rendah dari nilai Ka, warna yang tampak adalah warna HIn, dan jika pH lebih besar dari Ka, warna yang tampak adalah warna In–. Perubahan warna akan berkisar antara pH = pKa ±1. Kisaran angka ini disebut dengan trayek range pH indikator.
Contoh
Indikator metil jingga mempunyai traayek pH: 3,1 – 4,4 dengan perubahan warna dari merah ke kuning. Oleh karena itu, indikator metil jingga tersebut akan berwarna merah jika diteteskan pada larutan yang mempunyai pH < 3,1 dan akan memberikan warna kuning jika diteteskan pada larutan yang mempunyai pH > 4,4. Pada pH antara 3,1 – 4,4 warna metil jingga adalah campuran antara merah dan kuning, yaitu jingga.
Tabel jangkauan warna beberapa indikator asam basa
| Indikator Asam Basa | Perubahan warna | Trayek pH |
| Metil Jingga (MO) | Merah ke Kuning | 3,1 – 4,4 |
| Metil merah (MM) | Merah ke kuning | 4,4 – 6,2 |
| Lakmus | Merah ke biru | 4,5 – 8,3 |
| Bromtimol biru (BTB) | Kuning ke biru | 6,0 – 7,6 |
| Fenolftalein (PP) | Tak berwarna ke merah ungu | 8,3 – 10,0 |
Indikator tunggal hanya akan menunjuk hasil secara umum, misalnya suatu larutan ditetesi indikator PP berwarna merah, berarti larutan tersebut mempunyai pH > 8,3. Untuk mendapatkan hasil yang lebih teliti dapat digunakan beberapa indikator terhadap satu larutan.
Contoh soal
Suatu larutan akan memberikan warna kuning dengan indikator metil jingga dan metil merah, serta memberikan warna biru dengan indikator BTB. Sementara itu, dengan indikator PP tidak berwarna. Perkirakan nilai pH larutan tersebut.
Jawab:
Dengan metil jingga berwarna kuning= pH > 4,4
Dengan metil jingga berwarna kuning= pH > 6,2
Dengan BTB berwarna biru = pH > 7,6
Dengan PP tak berwarna = pH < 8,3
Jadi, pH larutan kira – kira = 7,6- 8,0
Perkirakan nilai pH ini juga tidak pasti tepat, namun nilai ini merupakan nilai yang lebih teliti dibandingkan jika hanya indikator tunggal. Akan tetapi, jika mengharapkan pengukuran nilai pH secara pasti dapat digunakan indikator Universal. Indikator universal merupakan campuran beberapa indikator yang dapat berubah pada setiap satuan nilai pH. Terdapat indikator universal ada yang berbentuk larutan atau kertas (stik) yaang dilengkapi dengan peta warna dan pH-nya.
Demikian ulasan mengenai indikator asam basa.. Semoga bermanfaat…..
Artikel Terkait
- asd
- asd
- Sinonim akulturasi adalah kontak kabudayaan #sinonim #bahasa #akulturaasi #bahasaindonesia #antonim
- Pada Suatu Pertemuan, Hadir 10 Orang yang Saling Berjabat Tangan. Banyaknya Jabat Tangan yang Terjadi Adalah... Jawaban dan Pembahasan
- Suku Kelima Suatu Barisan Aritmatika Adalah 22, Sedangkan Kesembilan Adalah 42. Suku Kelima Belas Sama Dengan... Jawaban dan Pembahasan
- Mata Uang yang Sering Digunakan Sebagai Alat Pembayaran dan Kesatuan Hitung Dalam Transaksi Ekonomi dan Keuangan Internasional Disebut...
- Kingdom yang Tidak Memiliki Dinding Sel... Jawaban dan Pembahasan
- Organel Sel yang Berperan Untuk Mendetoksifikasi Racun Adalah... Jawaban dan Pembahasan
- Diketahui Harga 4 kg Jeruk, 1 kg Semangka, dan 2 kg Apel Adalah Rp 54.000,00. Harga 1 kg Jeruk, 2 kg Semangka, dan 2 kg Apel Adalah Rp 43.000,00. Sedangkan Harga 3 kg Jeruk, 1 kg Semangka, dan 1 kg Apel Adalah Rp 37.500,00. Berapakah Harga 1 kg Semangka?
- Nilai Rataan Hitung dari Data 4 10 7 x 10 6 11 Adalah 8 Nilai x Adalah ...