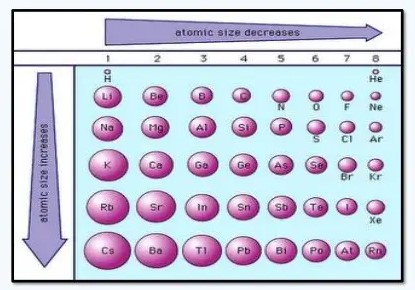
Jari Jari Atom

Jari-jari atom yaitu jarak dari inti atom ke orbital elektron yang paling luar yang stabil pada suatu atom dalam keadaan setimbang. Biasanya jarak itu diukur kedalam satuan pikometer atau angstrom. hal itu karna elektron-elektron senantiasa bergerak, maka untuk mengukur jarak dari inti atom kepadanya begitu sulit. Untuk itu digunakan beberapa cara yang lebih akurat
Kecenderungan Jari-Jari Atom
Jenis
Terdapat beberapa jenis jari-jari atom yang dipaka untuk menyatakan jarak dari inti atom ke lintasan stabil yang paling luar dari elektronnya, di antaranya yaitu :
- Jari-jari kovalen
- Jari-jari logam
- Jari-jari van der Waals
Ketiganya dipilih disebabkan oleh perbedaan dari sifat-sifat elemen yang diukur.
1. Jari-jari Kovalen
Jari-jari atom diukur memakai jari-jari kovalen untuk elemen-elemen yang mempunyai jenis ikatan kovalen. Pada umumnya elemen-elemen ini merupakan elemen-elemen non-logam. Secara teknis jarak yang diukur yaitu setengah dari jarak internuklir antara dua atom bertetangga terdekat dalam kisi kristal.
Jari-jari kovalen untuk elemen-elemen yang tidak bisa berikatan bisa diperkirakan dengan cara melakukan kombinasi jari-jari dari elemen-elemen yang bisa berikatan pada molekul untuk atom yang berbeda atau tak sama.
2. Jari-jari Logam
Jari-jari atom diukur memakai jari-jari logam untuk elemen-elemen yang termasuk pada elemen-elemen logam. Jari-jari logam yaitu setengah jarak dari jarak internuklir terdekat dari atom-atom dalam kristal logam.
3. Jari-jari Van Der Waals
Jari-jari atom diukur memakai jari-jari van der Waals untuk elemen yang atom-atomnya tak bisa saling berikatan. Contoh dari kelompok ini yaitu gas mulia, di mana dikatakan bahwa atom-atom dari elemen ini tidak termampatkan atau terpadatkan.
Dalam tabel periodik, jari-jari atom bertambah nilainya palu satu golongan ke bawah sejalan dengan bertambahnya lintasan elektron, dan berkurang kiri ke kanan karena dengan bertambahnya muatan inti – dengan perkecualian untuk golongan gas mulia.
Baca Juga :
Cara Menghitung Massa Atom Relatif (Ar) dan Massa Molekul Relatif (Mr)
Tabel Nilai Jari Jari Atom
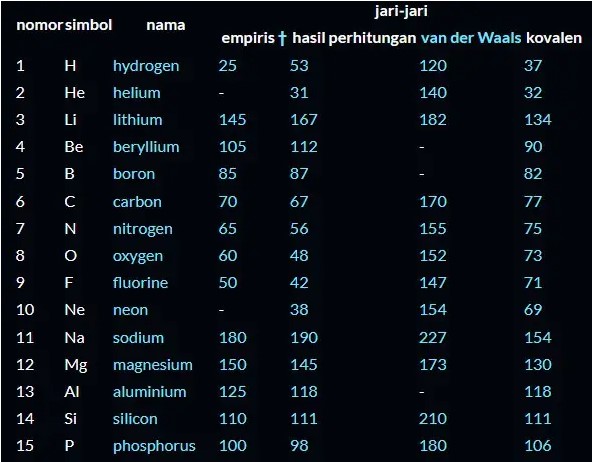
Keterangan:
Semua pengukuran ditulis dalam satuan pikometer (pm).
Faktor Yang Mempengaruhi Panjang Jari-Jari Atom
1. Jumlah kulit atom
Semakin banyak jumlah kulit yang dimiliki pada suatu atom, maka jari-jari atomnya juga semakin panjang. Nilai senyama atom Natrium lebih panjang daripada Litium, dikarenakan jumlah kulit yang dimiliki atom Natrium itu lebih banyak daripada atom Litium itu sendiri.
2. Muatan inti atom
Apabila jumlah kulit dari dua atom adalah sama banyak, maka yang berpengaruh pada panjangnya yaitu muatan inti atom. Makin banyak inti atom berarti makin besar juga muatan intinya dan gaya tarik inti atom pada elektron lebih kuat hingga elektron lebih mendekat ke inti atom.
Dalam tabel periodik bisa diamati bahwa:
- Didalam satu periode dari kiri kekanan semakin pendek, sedangkan unsur satu golongan dari atas kebawah semakin panjang. Hal ini bisa dijelaskan bahwasanya kecenderungan tersebut di akibatkan karna adanya gaya tarik inti terhadap suatu elekltron dan jumlah kulit elektron.
- Pada satu periode dari kiri ke kanan muatan inti semakin bertambah, sedangkan jumlah kulit elektronnya tetap, akibatnya yaitu gaya tarik inti pada elektron terluar makin kuat hingga menngakibatkan jarak elektron kulit terluar dengan inti makin dekat.
- Dalam satu golongan semakin kebawah jumlah kulit semakin banyak walaupun dalam hal ini jumlah muatan inti semakin banyak, Akan tetapi pengaruh bertambahnya jumlah kulit itu lebih besar daripada pengaruh muatan inti, mengakibatkan jarak elektron kulit terluar terhadap inti semakin jauh
Artikel Terkait
- Air Sangat Bermanfaat Khususnya Untuk Tubuh Kita, Karena 2/3 dari Tubuh Kita Terdiri dari Cairan. Tetapi Tidak Semua Air Itu Bisa Kita Konsumsi. Ada Syarat yang Harus Dipenuhi...
- Proses Alam yang Memecahkan Batuan Besar Menjadi Beberapa Bagian Batu Kecil dan Menghasilkan Perubahan Kimia pada Material Bahan Adalah...
- Campuran yang Tidak Dapat Dibedakan Antara Pelarut dengan Zat Terlarutnya Disebut? Jawaban dan Pembahasan
- Apa yang Dimaksud dengan Reduksi Bahan Berbahaya Dalam Kimia Hijau? Jawaban dan Pembahasan
- Kerajinan Atau Barang Jadi yang Terbuat dari Bahan Serat, Benang, Maupun Kain, yang Sebelumnya Merupakan Hasil Pengolahan Secara Kimia Disebut…
- Nilai Rata-rata Kimia Dalam Suatu Kelas Adalah 6,5. Jika Ditambah Nilai Siswa Baru yang Besarnya 9 Maka Rata-rata Menjadi 6,6. Banyak Siswa Semula...
- Zat Kimia yang Berfungsi Untuk Menghantarkan Rangsang Listrik Adalah? Jawaban Soal
- Cara yang Terbaik Untuk Melindungi Tiang Listrik dari Korosi Adalah ...
- Perubahan Materi di Bawah Ini yang Bukan Perubahan Kimia Adalah...
- Contoh Sifat Kimia dari Besi Adalah ...