Pengertian Sel Volta
Sel elektrokimia terdiri dari sepasang elektroda yang dicelupkan ke dalam suatu lelehan atau larutan ion dan dihubungkan dengan penghantar logam pada rangkaian luar. Sel elektrokimia dapat berupa sel volta atau sel galvani, dan sel elektrolisis.
Pengertian sel Volta
Sel volta adalah sel elektrokimia yang dapat menghasilkan energi listrik yang disebabkan oleh terjadinya reaksi redoks yang spontan. Sel Volta sering disebut juga sebagai sel Galvani karena Volta dan Galvani adalah ahli yang menemukan fenomena sel elektrokimia. Luigi Galvani (1737-1798), ahli fisiologi berkebangsaan Italia yang menyatakan adanya sifat listrik pada tulang hewan lewat percobaannya pada tulang katak. Sementara Alessandro Volta (1745-1827), ahli fisika yang juga berkebangsaan Italia, melakukan percobaan yang sama dan menyatakan bahwa aliran listrik yang terjadi adalah karena kontak logam yang tidak sama.
Reaksi redoks yang spontan, reaksi logam seng (Zn, Zinc) dengan larutan tembaga (II) sulfat (sumber ion Cu, atau copper)
Untuk lebih memahami sel volta, harus dipahami terlebih dahulu reaksi redoks spontan. Salah satu contoh reaksi redoks spontan adalah reaksi logam seng dengan larutan tembaga (II) sulfat. Jika logam seng yang berwarna abu-abu mengkilat dicelupkan ke dalam larutan tembaga (II) sulfat yang berwarna biru, lambat laun pada permukaan logam seng akan menempel logam tembaga yang berwana merah kecoklatan, sementara warna biru dari larutan akan memudar. Tembaga yang menempel pada logam seng berasal dari larutannya (ion tembaga (II) yang memberikan warna biru dalam pelarut air). Sementara itu, logam seng membentuk ionnnya yang larut dalam air, tetapi tidak memberikan warna pada larutannya. Reaksi tersebut dapat dinyatakan dengan persamaan:
Zn(s) + Cu2+(aq) → Zn2+(aq) + Cu(s)
Dalam persamaan reaksi diatas, dapat dilihat bahwa logam seng mengalami oksidasi membentuk ion seng (II). Reaksi ini disertai dengan pelepasan elektron:
Zn(s) → Zn2+(aq) + e–
Ion tembaga (II) membentuk logamnya dengan menerima elektron:
Cu2+(aq) + 2e– → Cu(s)
Jika reaksi dilangsungkan dengan cara di atas, elektron yang dilepaskan dari reaksi oksidasi langsung digunakan untuk reaksi reduksi pada permukaan logam seng. Elektron tidak berkesempatan untuk menghasilkan arus listrik yang dapat menghasilkan kerja.
Rangkaian Sel Volta
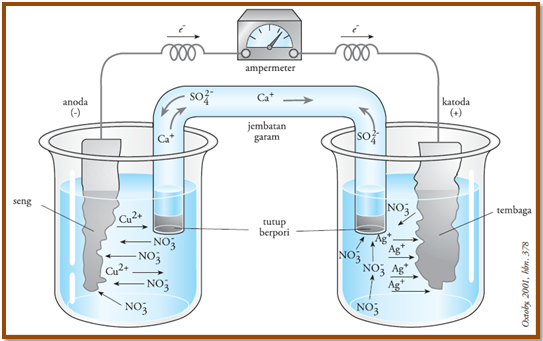
Salah satu jenis sel volta adalah sel Daniell. Dalam sel Daniell, elektron dirancang untuk mengalir pada rangkaian luar sehingga dapat menghasilkan kerja. Untuk maksud tersebut maka reaksi oksidasinya harus dipisahkan dari reaksi reduksinya sehingga membentuk sel seperti tampak pada gambar di bawah. Oh iya tak perlu dipermasalahkan ya antara sel Volta dengan sel Daniell. Jika disebutkan sel Daniel itu artinya sel Volta, karena sel Daniell merupakan contoh sel Volta.
Rangkaian Sel Volta:
Kedua larutan dihubungkan oleh jembatan garam yang berisi KCl.
Elektron mengalir dari elektroda Zn (sebagai anoda) ke elektroda Cu (sebagai katoda) melalui kawat eksternal.
Setengah sel yang satu terdiri dari logam seng (zinc) yang dicelupkan ke dalam larutan ZnSO4 dan setengah sel yang lainnya terdiri atas logam tembaga (copper) yang dicelupkan ke dalam larutan CuSO4. Jika kedua elektrodanya dihubungkan dengan rangkaian luar (misalnya kabel, kawat) maka akan dihasilkan arus listrik, yang dapat dibuktikan dengan bergeraknya jarum galvanometer yang dipasang pada rangkaian luar dari sel tersebut, ataupun dengan lam. Sel yang tampak di gambar sel volta di atas yang disebut juga sel Daniell, sesuai dengan nama orang yang mengembangkan alat tersebut. Ketika sel Daniell digunakan sebagai sumber listrik, terjad perubahan dari Zn menjadi Zn2+ yang bersifat dapat larut.
Zn(s) → Zn2+(aq) + 2e– (reaksi oksidasi)
Hal ini dapat diketahui dari semakin berkurangnya massa logam Zn. Di sisi lain, elektroda Cu semakin bertambah massanya karena terjadi pengendapan Cu dari Cu2+ dalam larutan.
Cu2+(aq) + 2e– → Cu(s) (reaksi reduksi)
Pada sel tersebut, elektroda Zn bertindak sebagai anoda dan elektroda Cu sebagai katoda. Pada sel elektrokimia, baik sel volta maupun sel elektrolisis, anoda adalah elektroda tempat terjadinya reaksi oksidasi dan katoda adalah tempat terjadinya reaksi reduksi. Untuk memudahkan mengingat perhatikan huruf pertama dari kata katoda dan kata reduksi. Huruf k dan r sama-sama merupakan huruf konsonan. Sementara huruf pertama dari kata anoda dan oksidasi adalah a dan o, sama-sama merupakan huruf vokal. Atau bisa juga untuk memudahkan mengingat, yaitu dengan menyingkatnya:
KRAO
K =Katoda, R= Reduksi, A= Anoda, O= Oksidasi
Ketika sel Daniell digunakan, terjadi arus elektron dari elektroda seng (Zn) ke elektroda tembaga (Cu) pada rangkaian luar. Kita ketahui bahwa dalam fisika ada konvensi yang menyatakan bahwa pada sumber arus, arus listrik mengalir dari kutub positif ke kutub negatif pada rangkaian luar, atau elektron mengalir mengalir dari kutub negatif ke kutub positif. Oleh karena itu, logam seng bertindak sebagai kutub negatif dan logam tembaga sebagai kitub positif. Bersamaan dengan itu pula, pada larutan dalam sel tersebut terjadi perpindahan sebagian ion Zn2+ dari kiri ke kanan. Hal ini terjadi karena dalam larutan sebelah kiri terjadi kelebihan ion Zn2+ dibandingkan dengan ion SO42- yang ada. Sementara itu, ion SO42- mengalir dari kanan ke kiri karena di sisi kanan kelebihan ion SO42- dibandingkan dengan ion Cu2+.
Reaksi total yang terjadi pada sel Daniell / sel volta adalah:
Zn(s) + Cu2+(aq) → Zn2+(aq) + Cu(s)
Reaksi tersebut merupakan reaksi redoks spontan yang dapat digunakan untuk memproduksi listrik melalui suatu rangkaian sel elektrokimia.
Demikian ulasan mengenai sel volta.. Semoga bermanfaat…..
Artikel Terkait
- Air Sangat Bermanfaat Khususnya Untuk Tubuh Kita, Karena 2/3 dari Tubuh Kita Terdiri dari Cairan. Tetapi Tidak Semua Air Itu Bisa Kita Konsumsi. Ada Syarat yang Harus Dipenuhi...
- Proses Alam yang Memecahkan Batuan Besar Menjadi Beberapa Bagian Batu Kecil dan Menghasilkan Perubahan Kimia pada Material Bahan Adalah...
- Campuran yang Tidak Dapat Dibedakan Antara Pelarut dengan Zat Terlarutnya Disebut? Jawaban dan Pembahasan
- Apa yang Dimaksud dengan Reduksi Bahan Berbahaya Dalam Kimia Hijau? Jawaban dan Pembahasan
- Kerajinan Atau Barang Jadi yang Terbuat dari Bahan Serat, Benang, Maupun Kain, yang Sebelumnya Merupakan Hasil Pengolahan Secara Kimia Disebut…
- Nilai Rata-rata Kimia Dalam Suatu Kelas Adalah 6,5. Jika Ditambah Nilai Siswa Baru yang Besarnya 9 Maka Rata-rata Menjadi 6,6. Banyak Siswa Semula...
- Zat Kimia yang Berfungsi Untuk Menghantarkan Rangsang Listrik Adalah? Jawaban Soal
- Cara yang Terbaik Untuk Melindungi Tiang Listrik dari Korosi Adalah ...
- Perubahan Materi di Bawah Ini yang Bukan Perubahan Kimia Adalah...
- Contoh Sifat Kimia dari Besi Adalah ...