Tekanan Osmosis
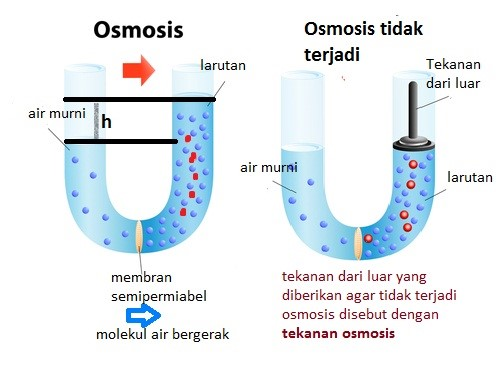
Osmosis ialah perpindahan molekul pelarut melalui selaput semipermiabel dari bagian yang lebih encer ke bagian yang lebih pekat atau dari bagian yang konsentrasi pelarut tinggi ke konsentrasi pelarut (misalnya air) rendah.
Membran semipermeabel harus mampu dilewati oleh pelarut, tetapi tidak oleh zat terlarut, yang mengakibatkan gradien tekanan sepanjang membran.
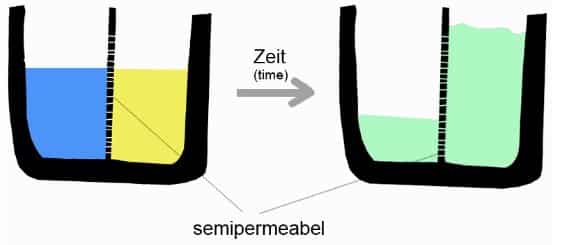
osmosis
Osmosis merupakan suatu fenomena alami, tetapi bisa dihambat secara buatan dengan cara meningkatkan tekanan pada bagian dengan konsentrasi pekat. Tekanan osmotik merupakan sifat koligatif, yang memiliki arti bahwa sifat ini bergantung pada konsentrasi zat terlarut, dan bukan pada sifat zat terlarut itu sendiri.
Rumus Osmosis
Besarnya tekanan Osmosis larutan oleh Van’t Hoff, dinyatakan dengan rumus:
∏ = M R T
Keterangan Rumus :
∏ = tekanan osmotik larutan (atmosfir)
M = molaritas larutan (mol/L)
R = konstanta gas = 0,08205 L atm mol-1 K-1
T = suhu mutlak (°C + 273) K
Dalam hubungannya dengan konsentrasi larutan Van’t Hoff menyimpulkan bahwa tekanan osmosis larutan akan semakin besar jika konsentrasi (Molar) dari zat terlarut semakin besar.
Faktor yang mempengaruhi Osmosis
- Suhu
Pergerakan molekul dipengaruhi pada suhu. Kadar resapan akan menjadi lebih cepat pada suhu yang tinggi dibandingkan dengan suhu yang rendah. - Ukuran molekul yang meresap
Molekul yang lebih kecil daripada garis pusat lubang membran akan meresap dengan mudah. - Ketebalan membran
Kadar resapan suatu molekul berkadar songsang dengan jarak yang harus dilaluinya. Berbanding dengan satu membran yang tebal, kadar resapan melalui satu membran yang tipis ialah lebih cepat. - Keterlarutan lipid
Molekul yang mempiliki keterlarutan yang tinggi meresap lebih cepat daripada molekul yang kelarutan yang rendah seperti lipid. - Luas permukaan membran
Kadar resapan menjadi cepat jika luas permukaan membran yang disediakan untuk resapan yaitu lebih besar.
Proses Terjadinya Osmosis
Osmosis ialah proses alami. Saat dua cairan konsentrasi yang berbeda dipisahkan pada sebuah membran semipermeabel, cairan mempunyai kecenderungan untuk bergerak dari konsentrasi yang lebih rendah ke konsentrasi yang lebih tinggi untuk keseimbangan potensial kimia.
Secara formal, reverse osmosis yaitu proses memaksa pelarut dari daerah konsentrasi zat terlarut tinggi melalui membran semipermeabel ke daerah konsentrasi zat terlarut rendah dengan cara menerapkan tekanan melebihi tekanan osmotik.
Proses terjadinya osmosis melalui simulasi komputer
Aplikasi terbesar dari reverse osmosis yaitu pemisahan air murni dari air laut dan air payau, air laut atau air payau bertekanan terhadap satu permukaan membran, menyebabkan transportasi garam-menipis air melintasi membran dan munculnya air minum dari sisi tekanan rendah.
Membran yang dipakai untuk reverse osmosis mempunyai lapisan padat dalam matriks polimer – baik kulit membran asimetris ataupun lapisan interfasial dipolimerisasi dalam membran tipis-film-komposit – di mana pemisahan terjadi
Osmosis Terbalik
Osmosis terbalik (Reverse osmosis) ialah suatu metode penyaringan yang mampu menyaring berbagai molekul besar dan ion-ion dari suatu larutan dengan cara memberi tekanan pada larutan saat larutan itu berada di salah satu sisi membran seleksi (lapisan penyaring).
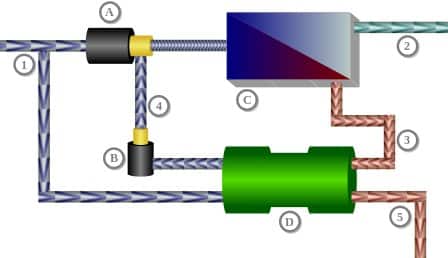
skema osmosis terbalik
Skema osmosis terbalik (desalinasi) memakai pertukaran tekanan.
1 : Aliran masuk air laut,
2 : Aliran air bersih flow (40%),
3 : Aliran konsentrasi (60%),
4 : Aliran air laut (60%),
5 : Konsentrat (pembuangan),
A : Aliran pompa tekanan tinggi (40%),
B : Pompa sirkulasi,
C : Satuan osmosis dengan membran,
D : Penukar tekanan
Proses itu menjadikan zat terlarut terendap di lapisan yang dialiri tekanan sehingga zat pelarut murni bisa mengalir ke lapisan berikutnya. Membran seleksi itu harus bersifat selektif yang artinya bisa dilewati zat pelarutnya (atau bagian lebih kecil dari larutan) tetapi tidak bisa dilewati zat terlarut seperti molekul berukuran besar dan ion-ion.
Contoh Osmosis
- Tempatkan kentang dalam air murni, Kentang akan membengkak dari waktu ke waktu. Hal ini disebabkan karena adanya konsentrasi yang lebih tinggi dari pati dan zat terlarut lainnya dalam sel kentang daripada di dalam air, sehingga air mengalir ke dalam sel kentang secara osmosis.
- Sel akar tanaman mengambil air dari tanah melalui osmosis
Contoh Osmosis Pada Tubuh
- Garam dan mineral dari air ditransfer melalui osmosis. Air mengalir melalui membran plasma sel dan karena konsentrasi osmosis air, glukosa dan garam dipertahankan dalam tubuh. Jadi filtrasi osmotik penting dalam mencegah kerusakan sel.
- Ikan air tawar menjaga keseimbangan cairan pada tubuh mereka melalui osmosis. Karena konsentrasi garam dalam tubuh ikan lebih tinggi dari air di sekitarnya, mereka tidak perlu minum air. Hal ini karena air spontan diserap oleh hadir garam dalam tubuh mereka
Contoh Osmosis Pada Kehidupan Sehari-hari
- Ketika tangan kita tenggelam pada cucian untuk waktu yang lama, kulit Akan terlihat membengkak. Ini adalah efek dari osmosis.
- Ketika kita menuangkan garam ke siput, air berdifusi dan siput menyusut akibat osmosis.
- Ketika kita memasak makanan dan menaruh saus di bagian cair dari piring Anda, beberapa bagian dari zat terlarut bergerak pada bagian padat dari makanan yang kita masak. Bagian padat bisa menjadi telur, sepotong daging tapi saus yang terbuat dari zat terlarut dan bukan air, sehingga akan pindah ke makanan.
Perbandingan Osmosis dan Difusi
- Osmosis terjadi saat ada membran semi-permeable, membran ini tidak dibutuhkan untuk terjadinya difusi.
- Keduanya bisa terjadi karena adanya perbedaan konsentrasi.
- Pada osmosis yang berpindah yaitu molekul-molekul pelarut, biasanya air. Sedangkan pada difusi yang berpindah yaitu molekul-molekul terlarut.
- Difusi bisa menyebar sampai jarak yang jauh, sedangkan osmosis terbatas pada jarak yang lebih dekat saja.
- Pada proses difusi, molekul-molekul terlarut bergerak dari konsentrasi tinggi ke konsentrasi rendah, sedangkan pada osmosis molekul-molekul pelarut mengalir secara kebalikannya.
- Keduanya termasuk transpor pasif sehingga tidak memerlukan energi eksternal agar kedua proses ini bisa terjadi.
- Difusi umumnya terjadi pada molekul-molekul gas, meski difusi juga bisa terjadi pada molekul padat-cair atau cair-gas.
- Osmosis hanya terjadi di antara dua larutan.
- Osmosis terjadi relatif lebih lambat jika dibandingkan dengan difusi.
Demikianlah penjelasan tentang osmosis, Semoga bermanfaat
Artikel Terkait
- asd
- asd
- Sinonim akulturasi adalah kontak kabudayaan #sinonim #bahasa #akulturaasi #bahasaindonesia #antonim
- Pada Suatu Pertemuan, Hadir 10 Orang yang Saling Berjabat Tangan. Banyaknya Jabat Tangan yang Terjadi Adalah... Jawaban dan Pembahasan
- Suku Kelima Suatu Barisan Aritmatika Adalah 22, Sedangkan Kesembilan Adalah 42. Suku Kelima Belas Sama Dengan... Jawaban dan Pembahasan
- Mata Uang yang Sering Digunakan Sebagai Alat Pembayaran dan Kesatuan Hitung Dalam Transaksi Ekonomi dan Keuangan Internasional Disebut...
- Kingdom yang Tidak Memiliki Dinding Sel... Jawaban dan Pembahasan
- Organel Sel yang Berperan Untuk Mendetoksifikasi Racun Adalah... Jawaban dan Pembahasan
- Diketahui Harga 4 kg Jeruk, 1 kg Semangka, dan 2 kg Apel Adalah Rp 54.000,00. Harga 1 kg Jeruk, 2 kg Semangka, dan 2 kg Apel Adalah Rp 43.000,00. Sedangkan Harga 3 kg Jeruk, 1 kg Semangka, dan 1 kg Apel Adalah Rp 37.500,00. Berapakah Harga 1 kg Semangka?
- Nilai Rataan Hitung dari Data 4 10 7 x 10 6 11 Adalah 8 Nilai x Adalah ...