Pengertian Redoks merupakan sebuah istilah yang menjelaskan adanya suatu perubahan bilangan oksidasi (keadaan oksidasi) atom-atom didalam sebuah reaksi kimia. Redoks ini merupakan singkatan dari reduksi serta oksidasi.
Adapun arti dari oksidasi ini ialah pelepasan elektron oleh sebuah molekul, atom serta ion, reaksi kenaikan bilangan oksidasi (biloks) serta juga reaksi pengikatan oksigen. Sedangkan untuk reaksi reduksi ini ialah reaksi penangkapan elektron, reaksi penurunan bilangan oksidasi (biloks) dan juga reaksi pelepasan oksigen.
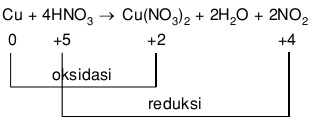
Redoks “reaksi Reduksi / Oksidasi” adalah istilah yang menggambarkan perubahan bilangan oksidasi (keadaan oksidasi) atom dalam reaksi kimia. Hal ini dapat berupa proses redoks yang sederhana seperti oksidasi karbon untuk menghasilkan karbon dioksida, atau reduksi karbon oleh hidrogen menghasilkan metana (CH4), atau dapat menjadi proses yang kompleks seperti oksidasi gula pada tubuh manusia melalui serangkaian kompleks transfer elektron.
Baca Juga : Materi Kelas X Redoks
Istilah redoks berasal dari dua konsep reduksi dan oksidasi. Dia bisa dengan mudah dijelaskan sebagai berikut:
Oksidasi ini menjelaskan pelepasan elektron oleh sebuah molekul, atom, atau ion
Reduksi ini menjelaskan penambahan elektron oleh sebuah molekul, atom, atau ion.
Meskipun cukup tepat untuk digunakan dalam berbagai tujuan, penjelasan ini tidak tepat benar. Oksidasi serta reduksi tepatnya merujuk pada perubahan bilangan oksidasi untuk transfer elektron yang sebenarnya tidak akan selalu terjadi.
Dengan demikian, oksidasi tersebut lebih baik didefinisikan sebagai peningkatan bilangan oksidasi, serta reduksi ialah sebagai penurunan oksidasi. Dalam prakteknya, transfer elektron ini akan selalu mengubah bilangan oksidasi, namun terdapat banyak reaksi yang diklasifikasikan ialah sebagai “redoks” walaupun tidak terdapat reaksi transfer elektron (misalnya yang melibatkan ikatan kovalen).
Baca Juga :
Reaksi Redoks: Rumus, Contoh Soal, Materi, Konsep
Reaksi non-redoks yang tidak melibatkan perubahan muatan formal (biaya resmi) dikenal dengan istilah reaksi metatesis.
Oksidator dan reduktor
Senyawa yang mempunyai kemampuan untuk dapat mengoksidasi senyawa lain dikatakan ialah sebagai oksidatif dan dikenal ialah sebagai oksidator atau juga agen oksidasi. Oksidan ini menghilangkan elektron dari senyawa lain, sehingga mengurangi sendiri. Oleh sebab itu ia “menerima” elektron, ia juga disebut ialah sebagai penerima elektron.
Ciri-ciri reaksi redoks
Dibawah ini terdapat beberapa ciri dari reaksi redoks didalam kehidupan sehari-hari yang diantaranya ialah sebagai berikut :
- Terdapat unsur bebas misalnya CI2 (klorin), Cu (Cuprum), O2 (oksigen).
- Terjadi suatu perubahan biloks (bilangan oksidasi).
- Terdapat reduktor (pereduksi) merupakan suatu zat yang mengalami oksidasi.
- Terdapat oksidator (pengoksidasi) merupakan suatu zat yang mengalami reduksi.
Fungsi redoks
Fungsi reaksi redoks didalam kehidupan sehari-hari ini akan dijelaskan dengan secara rinci diantaranya ialah sebagai berikut :
- Penggunaan lumpur aktif untuk mengolah limbah.
- Reaksi fotosintetis.
- Oksidasi makanan dalam sel.
- Mur serta baut diberi lapisan zinc yang mana di dalam lapisan itu terdapat proses oksidasi logam zinc dan juga reduksi pada bagian kation.
- Alat-alat dapur yang terbuat dari stainless steel tersebut tidak berkarat disebabkan karena permukaannya itu selalu dilapisi oksida akibat proses oksidasi yang continue.
- Memahami fenomena korosi logam serta cara pencegahannya.
- Pembuatan asam sulfat untuk keperluan industri.
- Pengolahan bijih-bijih logam di industri pertambangan.
- Metabolisme seluruh organ-organ tubuh menggunakan reaksi redoks.
Baca Juga :
Cara Penyetaraan Reaksi Redoks
Nah demikian lah penjelasan mengenai Pengertian Reaksi Redoks, Ciri Beserta Fungsinya, semoga apa yang dipaparkan dapat bermanfaat untuk anda. Terima kasih.

