Usaha Dalam Termodinamika

Dalam pembahasan termodinamika, besaran yang digunakan adalah besaran makroskopis suatu sistem, yaitu tekanan, suhu, volume, entropi, kalor, usaha, dan energi dalam.
Usaha yang dilakukan oleh sistem (gas) terhadap lingkungannya bergantung pada proses -proses dalam termodinamika, di antaranya proses isobarik, isokhorik, isotermal, dan adiabatik.
Usaha Sistem terhadap Lingkungannya
Pada pembahasan Bab sebelumnya, Anda telah mempelajari definisi usaha (W) yang dilakukan pada benda tegar, yaitu
W = F x s
Bagaimanakah cara menghitung usaha pada gas? Tinjaulah suatu gas yang berada dalam tabung dengan penutup berbentuk piston yang dapat bergerak bebas, seperti terlihat pada Gambar 2.
| Gambar 2. Ketika gas ideal di dalam tabung dipanaskan,gas tersebut memuai sehingga piston berpindah sejauh Δs. |
Ketika gas tersebut dipanaskan, piston akan berpindah sejauh Δs karena gas di dalam tabung memuai dari volume awal V1 menjadi volume akhir V2. Gaya yang bekerja pada piston adalah F = pA. Jika luas penampang piston (A) dan tekanan gas dalam tabung (P) berada dalam keadaan konstan, usaha yang dilakukan oleh gas dinyatakan dengan persamaan
W = pA Δs
Oleh karena A Δs = ΔV, persamaan usaha yang dilakukan gas dapat ditulis menjadi :
W = p ΔV (1–1)
atau
W = p(V2 – V1) (1–2)
dengan:
p = tekanan gas (N/m2),
ΔV = perubahan volume (m3), dan
W = usaha yang dilakukan gas (joule).
Baca Juga : Hukum, Sistem, dan Proses Termodinamika Lengkap
Nilai W dapat berharga positif atau negatif bergantung pada ketentuan berikut.
a. Jika gas memuai sehingga perubahan volumenya berharga positif, gas (sistem) tersebut dikatakan melakukan usaha yang menyebabkan volumenya bertambah. Dengan demikian, usaha W sistem berharga positif.
b. Jika gas dimampatkan atau ditekan sehingga perubahan volumenya berharga negatif, pada gas (sistem) diberikan usaha yang menyebabkan volume sistem berkurang. Dengan demikian, usaha W pada tersebut sistem ini bernilai negatif.
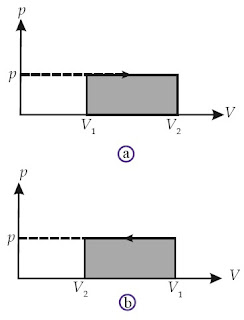
Usaha yang dilakukan oleh sistem dapat ditentukan melalui metode grafik. Pada Gambar 3a dapat dilihat bahwa proses bergerak ke arah kanan (gas memuai). Hal ini berarti V2 > V1 atau ΔV > 0 sehingga W bernilai positif (gas melakukan usaha terhadap lingkungan). W sama dengan luas daerah di bawah kurva yang diarsir (luas daerah di bawah kurva p –V dengan batas volume awal dan volume akhir)
Baca juga: Contoh Soal dan Pembahasan Tentang Termodinamika
Selanjutnya perhatikan Gambar 3b. Jika proses bergerak ke arah kiri (gas memampat), V2 < V1 atau ΔV < 0 sehingga W bernilai negatif (lingkungan melakukan usaha terhadap gas). W = – luas daerah di bawah kurva p–V yang diarsir.
| Gambar 3. (a) Grafik P–V suatu gas yang mengalami pemuaian (melakukan ekspansi) (b) Grafik P–V suatu gas yang mengalami pemampatan (diberi kompresi) |
Cobalah Anda tinjau kembali Persamaan (1–1). Dari persamaan tersebut dan grafik hubungan tekanan (p) terhadap (V) pada Gambar 3, Anda dapat menyimpulkan bahwa suatu sistem dikatakan melakukan usaha (W berharga positif) atau sistem diberi usaha (W berharga negatif), jika pada sistem tersebut terjadi perubahan volume ( ΔV).
Artikel Terkait
- Sejumlah gas ideal dipanaskan hingga suhunya 2 kali semula pada tekanan tetap dengan mengambil kalor dari sumber panas sebesar 300 j untuk melakukan kerja sebesar 250 j. selama siklus terjadi besarnya energi dalam yang dikerjakan oleh gas sebesar
- Suatu mesin Carnot, jika reservoir panasnya bersuhu 400 K akan mempunyai efisiensi 40%. Jika reservoir panasnya bersuhu 640 K, efisiensinya menjadi …. %.
- Mesin Carnot bekerja pada suhu tinggi 600 K mempunyai efisiensi 40%. Agar efisiensi mesin naik menjadi 75% dengan suhu reservoir rendah tetap, maka reservoir suhu tinggi harus dinaikkan menjadi ... ?
- Contoh Soal Termodinamika (Fisika SMA) - Go Royong With Agiv
- Hukum 3 Termodinamika (Fisika SMA) - Go Royong With Agiv
- Pengertian Termodinamika
- Contoh Soal dan Pembahasan Teori Kinetik Gas
- Teori Kinetik Gas dan Sifatnya
- Ringkasan Materi Suhu dan Kalor
- Ringkasan Materi Suhu dan Kalor