RUMUS ALKANA , DERET HOMOLOG ALKANA
Kali ini akan dibahas mengenai rumus alkana (rumus umum alkane) dan deret homolog alkana. O iya, alkana itu bahasa inggrisnya alkane ya
ALKANA
Setiap atom karbon mempunyai empat elektron valensi yang digunakan untuk membentuk ikatan kovalen dengan atom lainnya, yang digambarkan sebagai tangan ikatan. Jadi, atom karbon pada senyawa karbon selalu mempunyai empat tanga ikatan. Pada alkane, keempat tangan tersebut bila tidak digunakan untuk mengikat atom karbon yang lain akan digunakan untuk mengikat atom hidrogen.

metana
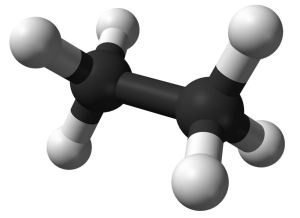
Penggantian (subsitusi) sebuah atom H yang mana pun pada gambar model molekul di atas dengan atom klorin, akan menghasilkan senyawa yang lain. Hal ini menunjukan bahwa semua atom H di dalam senyawa CH4 mempunyai kedudukan yang identik. Jika dua model molekul metana digabungkan, akan didapat molekul hidrokarbon dengan dua atom karbon didalamnya, seperti tampak pada gambar berikut.

etana
Baca Juga :
SIFAT KIMIA ALKANA & SIFAT FISIKA ALKANA
Rumus Alkana
Gambar tersebut menunjukan bahwa alkane yang terbentuk dari dua atom karbon akan mengikat enam atom hidrogen sehingga mempunyai rumus molekul C2H6. Jika penggantian atom hidrogen dengan atom karbon dilakukan terus menerus, akan didapat struktur seperti pada gambar di bawah.
| Jumlah atom C | Rumus struktur | Rumus Molekul |
| 1 | CH4 | CH4 |
| 2 | CH3– CH3 | C2H6 |
| 3 | CH3– CH2– CH3 | C3H8 |
| 4 | CH3– CH2– CH2– CH3 | C4H10 |
| 8 | CH3-CH2– CH2– CH2– CH2– CH2– CH2– CH3 atau
CH3(CH2)6CH3 | C8H18 |
| N | Rumus Alkana (rumus umum alkane) | CnH2n+2 |
Jadi, rumus alkana atau rumus umum molekul alkane adalah
CnH2n+2
Deret Homolog Alkana
Deretan rumus molekul alkane (tabel di bawah) menunjukan bahwa pada setiap anggota yang satu ke anggota yang berikutnya bertambah sebanyak CH2. Deret senyawa karbon yang demikian ini disebut deret homolog (deret homolog alkana). Deret homolog alkana mempunyai sifat – sifat berikut:
- Mempunyai rumus umum, untuk deret homolog alkana adalah CnH2n+2.
- Antara satu anggota ke anggota berikutnya mempunyai pembeda CH2.
- Selisih massa rumus antara satu anggota ke anggota berikutnya adalah 14.
- Semakin panjang rantai atom karbonnya, semakin tinggi titik didihnya.
Tabel yang menunjukan sebagian anggota deret homolog alkana dengan beberapa sifatnya.
| Jumlah atom C | Rumus Molekul | Nama | Titik lebur (oC) | Titik Didih (oC) | Massa jenis (g/cm3) | Wujud (suhu kamar) |
| 1 | CH4 | Metana | -181,9 | -163,9 | 0,466 | Gas |
| 2 | C2H6 | Etana | -183,2 | -88,5 | 0,572 | Gas |
| 3 | C3H8 | Propana | -189,6 | -42,0 | 0,585 | Gas |
| 4 | C4H10 | Butana | -138,3 | -0,4 | 0,601 | Gas |
| 5 | C5H12 | Pentana | -129,9 | 36,2 | 0,626 | Cair |
| 6 | C6H14 | Heksana | -94,9 | 69,1 | 0,660 | Cair |
| 7 | C7H16 | Heptana | -90,5 | 98,5 | 0,684 | Cair |
| 8 | C8H18 | Oktana | -56,7 | 125,8 | 0,703 | Cair |
| 9 | C9H20 | Nonana | -50,9 | 150,9 | 0,728 | Cair |
| 10 | C10H22 | Dekana | -29,6 | 174,2 | 0,730 | Cair |
| 11 | C11H24 | Undekana | -25,5 | 196,1 | 0,740 | Cair |
| 12 | C12H26 | Dodekana | -14,5 | 216,4 | 0,749 | Cair |
| 14 | C14H30 | Tetradekana | 5,9 | 253,5 | 0,763 | Cair |
| 18 | C18H38 | Oktadekana | 28 | 313,9 | 0,789 | Padat |
| 20 | C20H42 | Eikosana | 36,9 | 343,9 | 0,789 | Padat |
Demikian ulasan mengenai alkane, baik mengenai rumus alkana (rumus umum alkane) ataupun deret homolog alkana.
Semoga bermanfaat…..
Artikel Terkait
- asd
- asd
- Sinonim akulturasi adalah kontak kabudayaan #sinonim #bahasa #akulturaasi #bahasaindonesia #antonim
- Pada Suatu Pertemuan, Hadir 10 Orang yang Saling Berjabat Tangan. Banyaknya Jabat Tangan yang Terjadi Adalah... Jawaban dan Pembahasan
- Suku Kelima Suatu Barisan Aritmatika Adalah 22, Sedangkan Kesembilan Adalah 42. Suku Kelima Belas Sama Dengan... Jawaban dan Pembahasan
- Mata Uang yang Sering Digunakan Sebagai Alat Pembayaran dan Kesatuan Hitung Dalam Transaksi Ekonomi dan Keuangan Internasional Disebut...
- Kingdom yang Tidak Memiliki Dinding Sel... Jawaban dan Pembahasan
- Organel Sel yang Berperan Untuk Mendetoksifikasi Racun Adalah... Jawaban dan Pembahasan
- Diketahui Harga 4 kg Jeruk, 1 kg Semangka, dan 2 kg Apel Adalah Rp 54.000,00. Harga 1 kg Jeruk, 2 kg Semangka, dan 2 kg Apel Adalah Rp 43.000,00. Sedangkan Harga 3 kg Jeruk, 1 kg Semangka, dan 1 kg Apel Adalah Rp 37.500,00. Berapakah Harga 1 kg Semangka?
- Nilai Rataan Hitung dari Data 4 10 7 x 10 6 11 Adalah 8 Nilai x Adalah ...