Isomer Alkana
Isomer adalah peristiwa di mana suatu senyawa karbon mempunyai rumus molekul sama tetapi struktur berbeda.
Contoh
Senyawa dengan rumus molekul C4H10 mempunyai dua struktur yang berbeda, yaitu
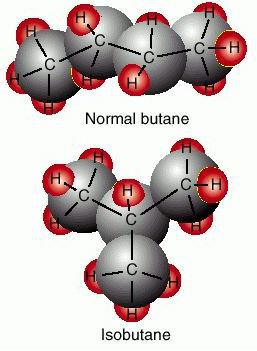
Atau jika diungkapkan dalam bentuk model molekul
Perbedaan antara senyawa n-butana (baca: normal butana) dengan metil propana adalah pada kerangka rantai karbonnya. Rantai n-butana tidak bercabang, sedangkan metil propana rantainya bercabang pada atom C-2. Perbedaan struktur kedua senyawa tersebut mengakibatkan kedua sifat, di mana titik didih n-butana adalah -0,4oC sedangkan titik didih metil propana adalah -11,6oC.
Semakin banyak jumlah atom karbon penyusun alkana, semakin banyak jumlah isomer alkana -nya.
Tabel: Jumlah isomer alkana dari beberapa senyawa
| Jumlah atom C | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 15 | 20 |
| Rumus molekul | C4H10 | C5H12 | C6H14 | C7H16 | C8H18 | C9H20 | C10H22 | C15H32 | C20H42 |
| Jumlah isomer | 2 | 3 | 5 | 9 | 18 | 35 | 75 | 4.347 | 366.319 |
Tabel berikut menunjukan perbedaan titik didih dan titik lebur dari isomer senyawa heksana.
Tabel: titik didih dan titik lebur isomer heksana (C6H14)
| Struktur | Nama | Titik didih (oC) | Titik lebur (oC) |
| CH3-CH2-CH2– CH2-CH2-CH3 | n-heksana | 69 | -95 |
 | 2-metil pentana | 60 | -154 |
 | 3-metil pentana | 63 | -118 |
 | 2,2-dimetil butana | 50 | -98 |
 | 2,2-dimetil butana | 58 | -129 |
Demikian ulasan mengenai isomer alkana. Semoga bermanfaat .....
Artikel Terkait
- Introductions (Perkenalan)
- asd
- asd
- Sinonim akulturasi adalah kontak kabudayaan #sinonim #bahasa #akulturaasi #bahasaindonesia #antonim
- Pada Suatu Pertemuan, Hadir 10 Orang yang Saling Berjabat Tangan. Banyaknya Jabat Tangan yang Terjadi Adalah... Jawaban dan Pembahasan
- Suku Kelima Suatu Barisan Aritmatika Adalah 22, Sedangkan Kesembilan Adalah 42. Suku Kelima Belas Sama Dengan... Jawaban dan Pembahasan
- Mata Uang yang Sering Digunakan Sebagai Alat Pembayaran dan Kesatuan Hitung Dalam Transaksi Ekonomi dan Keuangan Internasional Disebut...
- Kingdom yang Tidak Memiliki Dinding Sel... Jawaban dan Pembahasan
- Organel Sel yang Berperan Untuk Mendetoksifikasi Racun Adalah... Jawaban dan Pembahasan
- Diketahui Harga 4 kg Jeruk, 1 kg Semangka, dan 2 kg Apel Adalah Rp 54.000,00. Harga 1 kg Jeruk, 2 kg Semangka, dan 2 kg Apel Adalah Rp 43.000,00. Sedangkan Harga 3 kg Jeruk, 1 kg Semangka, dan 1 kg Apel Adalah Rp 37.500,00. Berapakah Harga 1 kg Semangka?