Apa Itu Hidrogen Fluorida?
Hidrogen fluorida digunakan dalam produksi aluminium dan chlorofluorocarbon, dan industri kimia dan dalam pengawetan stainless steel. Dan berikut adalah penjelasan tentang Hidrogen Fluorida semoga bermanfaat bagi yang membacanya.
Apa Itu Hidrogen Fluorida?
Hidrogen fluorida adalah senyawa kimia dengan rumus kimia HF. Gas atau cairan berwarna ini adalah sumber industri utama fluor , sering sebagai berair solusi yang disebut asam fluorida . Dengan demikian adalah prekursor banyak senyawa penting termasuk obat-obatan dan polimer (misalnya Teflon ).
HF secara luas digunakan dalam industri petrokimia sebagai komponen superasam . Hidrogen fluorida bisul di dekat suhu kamar, jauh lebih tinggi daripada lainnya halida hidrogen . Tidak seperti hidrogen halida lainnya, HF lebih ringan dari udara.
Hidrogen fluorida adalah gas yang sangat berbahaya, membentuk korosif dan penetrasi asam fluorida pada kontak dengan kelembaban. Gas juga dapat menyebabkan kebutaan oleh kerusakan yang cepat dari kornea .
Kimiawan Perancis Edmond Frémy (1814-1894) dikreditkan dengan menemukan anhidrat hidrogen fluorida ketika mencoba untuk mengisolasi fluorin , meskipun Carl Wilhelm Scheele disiapkan asam fluorida dalam jumlah besar pada tahun 1771, dan asam ini dikenal di industri kaca sebelum itu.
Struktur
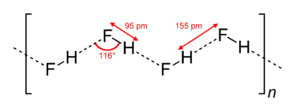
Meskipun molekul diatomik, bentuk HF relatif kuat antarmolekul ikatan hidrogen . Padat HF terdiri dari rantai zigzag molekul HF. Molekul HF, dengan H-F obligasi pendek 95 pm, terkait dengan molekul dengan antarmolekul jarak H-F dari 155 pm tetangga. Liquid HF juga terdiri dari rantai molekul HF, tapi rantai lebih pendek, yang terdiri rata-rata hanya lima atau enam molekul.
Perbandingan dengan Hidrogen Halida Lain
Hidrogen fluorida tidak mendidih sampai 20 ° C berbeda dengan hidrogen halida lebih berat yang mendidih antara -85 ° C (-120 ° F) dan -35 ° C (-30 ° F). ikatan hidrogen antara molekul HF menimbulkan tinggi viskositas dalam fase cair dan lebih rendah dari tekanan diharapkan dalam fase gas.
Hidrogen fluorida adalah larut dengan air (larut dalam proporsi ada), sedangkan hidrogen halida lain memiliki kesenjangan kelarutan besar dengan air. Hidrogen fluorida dan air juga membentuk beberapa senyawa dalam keadaan padat, terutama 1: 1 senyawa yang tidak meleleh sampai -40 ° C (-40 ° F), yang merupakan 44 ° C (79 ° F) di atas titik leleh HF murni.
Artikel Terkait
- asd
- asd
- Sinonim akulturasi adalah kontak kabudayaan #sinonim #bahasa #akulturaasi #bahasaindonesia #antonim
- Pada Suatu Pertemuan, Hadir 10 Orang yang Saling Berjabat Tangan. Banyaknya Jabat Tangan yang Terjadi Adalah... Jawaban dan Pembahasan
- Suku Kelima Suatu Barisan Aritmatika Adalah 22, Sedangkan Kesembilan Adalah 42. Suku Kelima Belas Sama Dengan... Jawaban dan Pembahasan
- Mata Uang yang Sering Digunakan Sebagai Alat Pembayaran dan Kesatuan Hitung Dalam Transaksi Ekonomi dan Keuangan Internasional Disebut...
- Kingdom yang Tidak Memiliki Dinding Sel... Jawaban dan Pembahasan
- Organel Sel yang Berperan Untuk Mendetoksifikasi Racun Adalah... Jawaban dan Pembahasan
- Diketahui Harga 4 kg Jeruk, 1 kg Semangka, dan 2 kg Apel Adalah Rp 54.000,00. Harga 1 kg Jeruk, 2 kg Semangka, dan 2 kg Apel Adalah Rp 43.000,00. Sedangkan Harga 3 kg Jeruk, 1 kg Semangka, dan 1 kg Apel Adalah Rp 37.500,00. Berapakah Harga 1 kg Semangka?
- Nilai Rataan Hitung dari Data 4 10 7 x 10 6 11 Adalah 8 Nilai x Adalah ...